La fibrillation auriculaire
Aurélie Perrault, infirmière, Hôpital Simone Veil, Centre Hospitalier de Troyes
Décembre 2022
La fibrillation atriale (FA), ou fibrillation auriculaire, est le trouble du rythme cardiaque le plus fréquent. Sa prévalence, en constante augmentation, et la morbi-mortalité associée, représentent une charge pour les systèmes de santé, les équipes pluridisciplinaires et les patients. Ces dernières décennies, le développement des connaissances scientifiques et les progrès technologiques ont fortement amélioré la prise en charge de cette pathologie. Les sociétés savantes, publient régulièrement des recommandations dont les plus récentes, éditées en 2020 par la Société Européenne de Cardiologie (ESC), ont guidé l’écriture de cet article.
Epidémiologie
La prévalence de la FA dans la population adulte est estimée entre 2 et 4%1 et au-delà de 10% pour les plus de 80 ans2. Ces indicateurs sont en augmentation en raison de l’accroissement de la longévité et des nouvelles technologies qui facilitent le dépistage. La prévalence augmente avec l’âge, la présence d’une cardiopathie et chez les patients présentant certains facteurs de risques tels que l’HTA, l’apnée du sommeil, l’obésité, le diabète et la consommation d’alcool. Cette pathologie a un impact médico-économique majeur puisque 30% des patients atteints de FA ont au moins 1 hospitalisation par an3, 60 % d’entre eux ont une qualité de vie significativement altérée4 et le risque de mortalité est multipliée par 3,55.
Définition
La FA est caractérisée par un rythme cardiaque irrégulier, le plus souvent rapide, d’origine auriculaire. L’activité électrique rapide et anarchique des oreillettes se situe aux environs de 350 à 600 battements/min. Le nœud auriculoventriculaire joue un rôle de filtre protecteur du ventricule, toutes les impulsions auriculaires ne sont pas transmises et la fréquence des transmissions est modulée par le système nerveux autonome et le cas échéant, par les traitements bradycardisants.
Physiopathologie
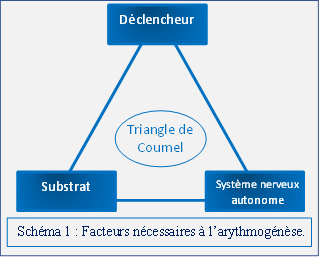
D’un point de vue physiopathologique et électrophysiologique, la FA se caractérise par la présence d’une activité fibrillatoire (contraction rapide et non coordonnée des cellules myocardiques auriculaires) dont le déclenchement et l’entretien sont dépendants de trois facteurs. Communs à toute arythmie le déclencheur, le substrat et le système nerveux autonome ont été schématisés par le Pr Philippe Coumel en 1987 comme facteurs nécessaires à l’arythmogénèse (cf. schéma 1).
Dans le cas de la FA, le déclencheur correspond aux extra-systoles auriculaires prenant principalement leur origine dans les veines pulmonaires tel que décrit par le Pr Haissaguerre en 1998. Ce battement prématuré auriculaire, prend le pas sur le déclenchement sinusal et vient amorcer l’arythmie rendue possible par un substrat propice.
Le substrat quant à lui correspond au tissu auriculaire. La distension de l’oreillette et les zones de fibrose constituent un substrat électrophysiologique et anatomique propice à l’initiation et à la pérennisation de la FA qui elle-même favorise le remodelage auriculaire, soit la constitution potentielle d’un cercle vicieux.
Enfin, le système nerveux autonome ainsi que les facteurs électrolytiques et métaboliques viendront impacter le déclenchement et la pérennisation de l’arythmie.
Classification de la fibrillation atriale :
La combinaison entre la composante temporelle de l’arythmie et l’attitude thérapeutique adoptée, donne lieu à la classification suivante :
- Paroxystique : FA d’une durée inférieure à 7 jours.
- Persistante : FA d’une durée supérieure à 7 jours.
- Persistante de longue durée : FA continue supérieure à 12 mois.
- Permanente : attitude thérapeutique d’acceptation de la FA.
Présentation clinique, dépistage et diagnostic
Les circonstances de découverte et de dépistage sont variables. Les symptômes les plus fréquents sont les palpitations, la dyspnée et l’asthénie mais elle peut aussi se manifester par des douleurs ou oppressions thoraciques, une faible tolérance à l’effort, des lipothymies, plus rarement des syncopes et une perturbation du sommeil. Cependant, le patient peut être asymptomatique ce qui retarde le diagnostic. Dans ce cas, la FA peut être découverte fortuitement lors d’une consultation guidée ou non par la présence de facteurs de risque, ou par le patient lui-même lors d’une prise de pouls. Enfin, elle peut être révélée par la survenue d’une complication telle qu’un accident vasculaire cérébral (AVC) ou de l’insuffisance cardiaque (IC).
Selon les recommandations de 2020 de la Société Européenne de Cardiologie (ESC), le diagnostic repose sur un rythme cardiaque irrégulier sans onde P visible, objectivé soit sur un électrocardiogramme 12 dérivations, soit sur un tracé 1 dérivation, de plus de 30 secondes. La gamme des outils diagnostics s’est élargie : électrocardiogramme, holter ECG, enregistreur d’évènements mais aussi depuis peu certains outils connectés, permettant un enregistrement immédiat au moment des symptômes, augmentant la rentabilité diagnostique. Les moniteurs cardiaques implantables et prothèses cardiaques thérapeutiques (stimulateurs et défibrillateurs cardiaques) représentent une opportunité diagnostique et apportent un gain en termes de précocité lorsqu’ils sont combinés à un télésuivi. Dans ce dernier cas, la FA est dite infraclinique si elle est asymptomatique et n’est pas documentée stricto sensu par un électrocardiogramme conforme aux recommandations.
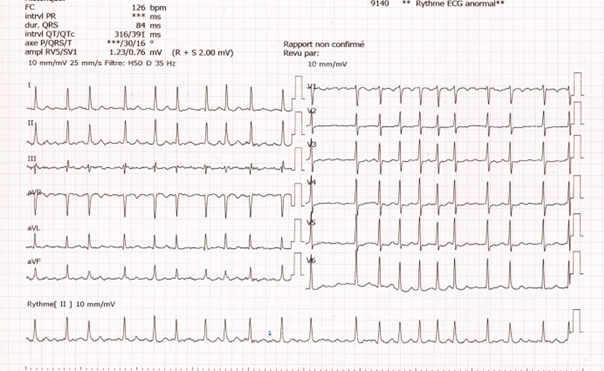
Electrocardiogramme en fibrillation atriale :
Rythme cardiaque irrégulier, absence d’onde P, présence d’atriogrammes correspondant à l’activité fibrillatoire rapide des oreillettes.
Les complications de la fibrillation atriale
La perte de la systole atriale, le remodelage auriculaire et la dysfonction ventriculaire liée à la tachycardie sont les causes principales des manifestations cliniques et des complications. La perte de systole atriale diminue le débit cardiaque et est également responsable de la stase sanguine atriale, propice à la formation de thrombus à risque embolique artériel notamment au niveau cérébral.
La dysfonction diastolique et systolique du ventricule gauche est responsable de l’insuffisance cardiaque. Cette dernière peut être cause ou conséquence de la FA. En tout état de cause, FA et dysfonction ventriculaire gauche se potentialisent.
Le dépistage précoce permet une prise en charge rapide pour limiter l’installation, la pérennisation de la FA et ses complications.
La prise en charge thérapeutique du patient atteint de fibrillation atriale
Les directives de l’ESC de 2020 précisent que « La complexité de la FA nécessite une approche multidimensionnelle, holistique et multidisciplinaire de la prise en charge des patients, avec leur implication active ». Celle-ci s’articule autour des thérapeutiques médicamenteuses et interventionnelles associées à la correction des facteurs de risques et comorbidités.
Schéma : Prise en charge des patients atteints de FA.
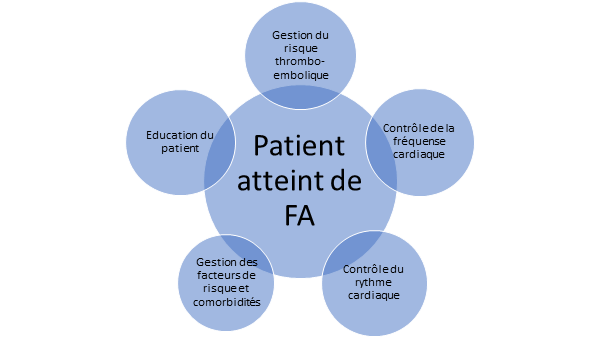
- Gestion du risque thromboembolique
Les anticoagulants oraux ont pour but de prévenir les accidents thrombo-emboliques, le plus souvent sous forme d’AVC ischémiques. Leur prescription est adaptée aux risques thromboembolique et hémorragique du patient.
Le score CHA2DS2-VASc est le plus connu et admis par les Sociétés Savantes pour évaluer le risque thromboembolique. Il prend en compte les facteurs suivants : insuffisance cardiaque congestive, HTA, âge ≥ 75 ans, diabète, antécédent d’accident vasculaire, maladie vasculaire, âge ≥ 65 ans et le sexe féminin. Chaque facteur représente 1 point, hormis l’âge ≥ 75 ans et l’antécédent d’accident vasculaire qui comptabilisent 2 points. Plus le score est élevé plus le risque d’AVC est important.
Concernant l’évaluation du risque hémorragique plusieurs scores sont utilisés, tel que le score HAS-BLED adopté par l’ESC, dans le but de repérer les facteurs de risques hémorragiques modifiables ainsi que les contre-indications absolues aux anticoagulants oraux. Pour les patients à haut risque embolique et hémorragique, la mise en place d’un dispositif de fermeture de l’auricule gauche (point de départ habituel des thrombi) peut être envisagée.
L’utilisation des AOD (Anticoagulants Oraux Directs) s’est largement répandue, les études ayant montré de façon concordante une diminution du risque hémorragique cérébral avec ces anticoagulants dont l’efficacité est au moins égale à celle des anticoagulants traditionnels (AVK) et dont l’usage est facilité pas la stabilité de l’anticoagulation.
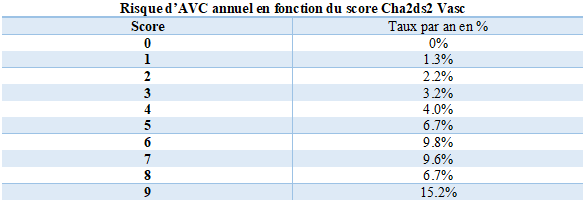
Référence : European Heart Rythm Association. Guidelines for the management of atrial fibrillation :
the Task Force for the Management of Atrial Fibrillation of the European Society of Cardiology (ESC) Eur Heart J. 2010 ;31(19) :2369-2429
-
Contrôle de la fréquence cardiaque
Le contrôle de la fréquence cardiaque a pour objectif d’améliorer la tolérance clinique de la FA. Il est particulièrement pertinent pour les patients en FA permanente. Les thérapeutiques utilisées pour ralentir la FA sont les bétabloquants, la digoxine et les inhibiteurs calciques bradycardisants. Le choix thérapeutique est guidé par les symptômes, la tolérance clinique, les comorbidités, les contres indications éventuelles à un traitement.
En cas d’échec du traitement pharmacologique, l’ablation du nœud auriculo-ventriculaire peut être envisagée après l’implantation d’un stimulateur cardiaque, de préférence bi-ventriculaire qui permet une contraction synchronisée des parois des ventricules droits et gauches.
- Contrôle du rythme cardiaque
Le contrôle du rythme cardiaque a pour but de restaurer ou de maintenir le rythme sinusal avec plusieurs objectifs : corriger les symptômes, prévenir la pérennisation de la pathologie, éviter les complications hémodynamiques et améliorer la qualité de vie du patient. Différentes approches thérapeutiques sont possibles : traitement anti-arythmique, cardioversion médicamenteuse ou électrique, ablation de fibrillation atriale.
La cardioversion médicamenteuse fait appel aux traitements anti-arythmiques. La cardioversion électrique permet une restauration immédiate du rythme sinusal, l’enjeu étant de pérenniser ce dernier, ce qui nécessite souvent le recours aux anti arythmiques. Ces deux méthodes peuvent être combinées.
L’ablation de fibrillation atriale est indiquée chez les patients symptomatiques soit après échec ou intolérance des anti arythmiques soit en première intention à la demande du patient ou en cas d’insuffisance cardiaque. La FA paroxystique et la FA persistante sans facteurs de risques de récidive post ablation constituent les meilleures indications de cette thérapeutique. Le patient, impliqué dans la prise de décision, est informé des bénéfices et des risques potentiels. La stratégie interventionnelle repose sur l’isolation électrique des veines pulmonaires, foyer d’extrasystoles responsables du déclenchement de l’arythmie. L’isolation électrique s’effectue par la création d’une cicatrice circonférentielle sur le pourtour des veines pulmonaires. Les moyens technologiques évoluent et se diversifient, ainsi les opérateurs peuvent utiliser un cathéter de radiofréquence guidé par un système de cartographie 3D, un ballon de cryothérapie, un système à énergie laser guidé par une caméra vidéo miniature, et l’électroporation, technique émergente. D’autres zones du substrat arythmogène auriculaire peuvent être ciblées en fonction des éléments électrophysiologiques identifiés notamment dans la FA persistante.
Bien que moins efficaces que l’ablation et responsables d’effets pro-arythmogènes et hémodynamiques, les traitements médicamenteux anti-arythmiques ont également une place importante dans la prise en charge de la FA que ce soit de façon isolée ou en post ablation, ou associés aux autres stratégies de contrôle du rythme. Leur efficacité est imparfaite pour maintenir le rythme sinusal, ils visent à réduire plutôt qu’à éliminer les récidives de FA et participent à la réduction des symptômes liés à l’arythmie. L’échec d’un traitement ou une mauvaise tolérance clinique peut nécessiter une modification du traitement. Ainsi, le clinicien qui adapte la thérapeutique en tenant compte de la tolérance et du terrain, utilise en pratique différents anti arythmiques tels que l’Amiodarone ou la Flécaïne, associée à un traitement bradicardisant.
- Détection et prise en charge des facteurs de risque modifiables et des comorbidités associées.
Le traitement des facteurs de risque y compris ceux liés au mode de vie et des comorbidités associées, est intégré dans le parcours de soin du patient et réalisé par une équipe pluridisciplinaire. Leur prise en charge, si elle est efficace et pérenne, diminue le risque de récidive, notamment de FA persistante et en tout état de cause, la charge en FA.
Les principales comorbidités justifiant une prise en charge sont :
- L'hypertension artérielle, facteur de risque le plus courant associé au développement de la FA mais aussi associée à un risque accru de complications hémodynamiques, emboliques et hémorragiques.
- Le diabète. La prévalence de la FA est au moins deux fois plus élevée chez les patients diabétiques.
- Le syndrome d’apnées obstructives du sommeil est très répandu chez ces patients. Un traitement approprié diminue le risque de récidive.
- Les pathologies cardiaques aigües et chroniques telles que l’infarctus du myocarde, l’insuffisance cardiaque et les cardiopathies valvulaires augmentent l’incidence de la FA.
- Les autres comorbidités en causes sont notamment l’insuffisance rénale chronique, les pathologies pulmonaires aigües et chroniques et l’hyperthyroïdie.
D’autres facteurs nécessitent une modification du mode de vie, tels que l’obésité, la consommation excessive d’alcool, la sédentarité. L’exercice physique modéré a des effets bénéfiques sur la santé cardiovasculaire et diminue le risque de FA mais paradoxalement la pratique d’une activité sportive intense à long terme ou d’endurance excessive augmente l’incidence de la FA.
- L’information et l’éducation du patient autour de sa pathologie et de ses facteurs de risques.
La prise en charge intégrée par un parcours de soins individualisé et coordonné, l’implication du patient par les professionnels de santé dans la prise de décisions partagées ainsi que l’éducation concernant sa pathologie, sa prise en charge et ses facteurs de risques améliorent l’adhésion aux choix thérapeutiques, l’observance, le mode de vie, la satisfaction du patient et finalement le pronostic.
L’éducation thérapeutique est une démarche qui nécessite la réalisation d’un bilan éducatif initial, évaluant les connaissances et les représentations du patient concernant sa pathologie, son ressenti, son environnement social et son profil éducatif. Le patient définit ensuite ses objectifs, les évalue lors des consultations et en fixe de nouveaux. Il s’agit d’une démarche d’accompagnement dont le but est notamment de repérer les éléments bloquants. L’intervention d’une infirmière spécialisée en éducation thérapeutique peut être envisagée. Certains centres, proposent une prise en charge en collaboration entre cardiologue et infirmière en pratique avancée spécialisée dans la prise en charge de la FA, le suivi des facteurs de risque et la coordination du parcours patient.
Exemple de prise en charge d’un patient atteint de FA:
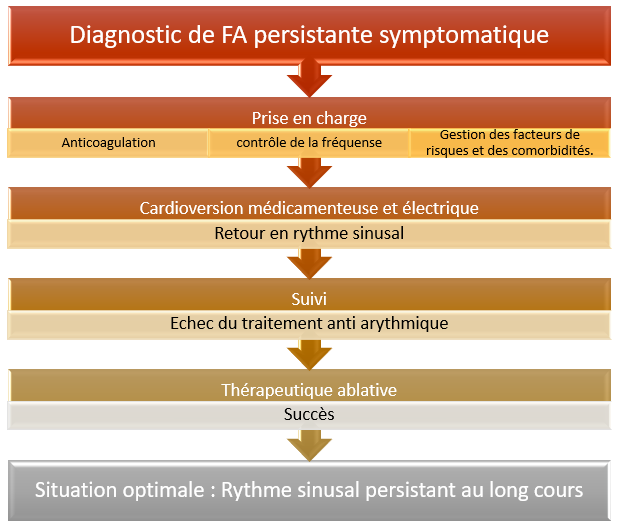
Conclusion :
La fibrillation atriale est une pathologie fréquente et lourde pour les systèmes de santé et les patients. Les progrès de la rythmologie interventionnelle et de l’imagerie médical ont révolutionné la prise en charge des patients avec l’avènement des thérapeutiques ablatives de plus en plus efficaces et sures. L’apparition d’outils numériques de dépistage ouvre un champ d’exploration dont l’enjeu principal est la prévention de l’AVC et de l’IC. Les stratégies de prise en charge en pleine mutation positionnent le patient au centre d’un parcours de soins individualisé et coordonné, au sein d’une équipe interdisciplinaire dont l’objectif est d’optimiser la prise en charge.
Références :
- Lignes directrices 2020 pour la prise en charge de la fibrillation auriculaire, Directives de pratique clinique de l'ESC (European Society of Cardiology, 20 août 2020.
- Cardio online SFC, « Recommandations ESC 2020 sur le diagnostic et la prise en charge de la fibrillation atriale », Christophe Leclerc.
- Précis de rythmologie de la société française de cardiologie, sous la direction de N. Saoudi et J-C Deharo, sauramps medical, 2004.
- Film de présentation des travaux de Michel Haïssaguerre, Centre Hospitalier Universitaire de Bordeaux. 24 avril 2015.
- 1. Statistiques sur les maladies cardiaques et les accidents vasculaires cérébraux - Mise à jour 2019 : un rapport de l’American Heart Association. Circulation : Vol.139, N°10.
- 2. Epidémiologie de la fibrillation auriculaire en France : extrapolation des données épidémiologiques internationales à la France et analyse des données françaises d'hospitalisation. Archives des maladies cardiovasculaires Volume 104, numéro 2, février 2011 , pages 115-124.
- 3. Facteurs d’hospitalisation chez les patients atteints de fibrillation auriculaire : résultats du registre des résultats pour un traitement informé de la fibrillation auriculaire (ORBIT-AF). American Heart Journal. Volume 167, Numéro 5, mai 2014.
- 4. Association entre les symptômes de la fibrillation auriculaire, la qualité de vie et les résultats pour les patients : résultats du registre des résultats pour un traitement informé de la fibrillation auriculaire (ORBIT-AF). Circulation : Cardiovascular Quality and Outcommes. Juillet 2015 Juil; Vol 8 ; n°4 : 393-402.
- 5. Différences et similitudes entre les sexes dans l’épidémiologie de la fibrillation atriale, les facteurs de risque et la mortalité dans les cohortes communautaires. 16 octobre 2017. Circulation : Vol.136, N°17.
Vous devez être connecté pour poster un commentaire