Les troubles du rythme à l'âge pédiatrique
Dr Alice MALTRET, Hôpital Marie Lannelongue-M3C, GHPSJ, Université Paris Saclay
Mars 2022
-
Combien d’enfant font des troubles du rythme et à quel âge ?
La fréquence des troubles du rythme de l’enfant est mal connue car on pense qu’un certain nombre de troubles du rythme paroxystiques passent inaperçus. On estime à 1 sur 1000 à 2500 le nombre d’enfant faisant des troubles du rythme.
L’enfant peut faire des troubles du rythme à tout âge. On distingue cependant 3 périodes dites « à risque » pendant lesquels les troubles du rythme sont le plus souvent diagnostiqués. Il s’agit des premiers mois de vie. Les troubles du rythme peuvent débuter pendant les derniers mois de grossesse, récidiver ou persister après la naissance ou enfin être découvert durant la période néonatale. Les troubles du rythme persistants, diagnostiqués pendant la grossesse, peuvent faire l’objet d’un traitement par voie trans-placentaire. Cela consiste à donner des antiarythmiques qui passe la barrière placentaire, et vont ainsi avoir une action sur le rythme cardiaque du fœtus. Le but de ce traitement est de réduire ou de ralentir le trouble du rythme afin que l’enfant à naitre ne développe pas d’insuffisance cardiaque pendant la vie intra-utérine.
Chez les enfants n’ayant pas de cardiopathie la seconde période à risque est l’âge scolaire à partir de 5-6 ans. Enfin, à tous âges, les enfants avec une malformation cardiaque congénitale sont plus à risque de faire des troubles du rythme, particulièrement dans la période post-opératoire.
-
Quels troubles du rythme fait l’enfant ?
Les arythmies de l’enfant sans cardiopathies sont presque essentiellement des troubles du rythme supraventriculaires. Le mécanisme principal est la réentrée sur une voie accessoire visible à l’ECG de base (syndrome de Wolff Parkinson White) ou non (Voie accessoire cachée de conduction rétrograde exclusive) qui explique jusqu’à 80% des troubles du rythme dans les premières années de vie. Cette proportion diminue avec l’âge au profit des réentrées intra-nodales qui s’observent, chez l’enfant, essentiellement après l’âge de 6 ans. Les flutters, par macro réentrée intra atrial, sont beaucoup plus rare que chez l’adulte et surviennent essentiellement dans la période périnatale chez les enfants n’ayant pas de cardiopathie congénitale ou, plus tard dans la vie, après une chirurgie de cardiopathie congénitale. La fibrillation atriale est exceptionnelle chez l’enfant.
Il est courant de constater des extrasystoles supra-ventriculaires (hyperexcitabilité supra ventriculaire) ou ventriculaire sur les derniers monitorings avant l’accouchement ou lors des examens de maternité du nouveau-né. Les ESV sont parfois en salves soutenues, on parle de RIVA ou Rythme Idio Ventriculaire Accéléré, quand la fréquence en QRS larges n’excède pas 10 à 15% de la fréquence attendue en rythme sinusal. Ces accès en QRS larges sont généralement bénins si l’échographie cardiaque ne retrouve pas d’anomalie architecturale ou fonctionnelle.
Les authentiques tachycardies soutenues par foyer ectopique persistant au-delà des premiers mois de vie sont plus rare à l’âge pédiatrique.
Les tachycardies ventriculaires (TV) peuvent être méconnues chez l’enfant quand le QRS n’est pas très élargies. Les TV sont très peu fréquentes et peuvent être confondus avec une tachycardie supra ventriculaire avec aberration de conduction. C’est le cas de la tachycardie fasciculaire gauche qui concernent les enfants dès l’âge de 3 ans. Cette tachycardie est volontiers déclenchée par l’effort ou la fièvre et se caractérise par une tachycardie dont les QRS sont peu élargis avec un aspect de retard droit, axe ascendant. Les troubles du rythme ventriculaire survenant après une chirurgie cardiaque sont moins fréquents à l’âge pédiatrique qu’à l’âge adulte. Ils ne doivent pourtant pas être méconnus car ils mettent en jeu le pronostic vital.
-
Quelle est la présentation clinique des tachycardies de l’enfant ?
La présentation clinique des tachycardies de l’enfant dépend de son âge et de sa capacité à exprimer ces symptômes. Dans les premiers mois et premières années de vie, avant le développement du langage, les signes cliniques de tachycardie sont frustres et rendent le diagnostic difficile. Les parents rapportent parfois des difficultés alimentaires, un changement de teint, une apathie inhabituelle qui traduit un début d’insuffisance cardiaque. Si la tachycardie reste méconnu et perdure, le diagnostic peut être fait au stade de défaillance cardiaque nécessitant la mise sous assistance circulatoire.
Lorsqu’il est en âge de s’exprimer et toujours selon son âge, la plainte fonctionnelle est plus ou moins précise. L’enfant exprime parfois au premier plan des maux de ventre, une difficulté respiratoire et la notion de « cœur qui court dans la poitrine » ou « cœur qui veut sortir » n’arrive qu’au second plan.
Enfin, chez l’enfant plus grand, la description d’un « cœur qui tape fort et/ou vite » n’est pas toujours lié à un authentique trouble du rythme paroxystique. L’interrogatoire doit alors préciser les circonstances de déclenchement, le contexte psychologique et familial ainsi que le mode de début et de fin des accès. Si certaines anamnèses évoquent clairement un éréthisme cardiaque ou des symptômes de désadaptation cardiaque, c’est l’ECG per critique qui permet de préciser le diagnostic. L’Holter ECG peut être utile en cas de symptôme quotidien. Pour les accès sporadiques, les outils actuels, tel que les montres connectées, permettent d’enregistrer des tracés d’une dérivation à la demande.
-
Comment évoluent les troubles du rythme de l’enfant ?
L’évolution des troubles du rythme de l’enfant est différente de celle des adultes. Après un premier accès de tachycardie par réentrée sur une voie accessoire dans la période néonatale, un enfant à une chance sur 2 de refaire un nouvel accès dans la première année de vie. Ce risque diminue passé cette période avec une « lune de miel » de plusieurs années sans récidive de tachycardie chez 90% des enfants. A l’entrée dans l’adolescence, les tachycardies vont de nouveau se manifester chez certains d’entre eux. Le pourcentage de patients qui refont une tachycardie augmente avec la durée du suivie. Le taux est de 60% de récidive à 26ans.
L’évolution du flutter néonatal est tout à fait singulier car, en l’absence de cardiopathie associée, les récidives sont rarissimes.
L’hyperexcitabilité atriale et ventriculaire néonatale a, elle aussi, une évolution spontanée le plus souvent favorable. En effet, on l’attribue à une immaturité électrophysiologique qui s’amende dans les premières semaines de vie.
Sur le même principe les tachycardies par automatisme anormal à l’étage atrial, diagnostiqué avant l’âge de 3 ans, ont près de 80% de chance de rentrer dans l’ordre spontanément.
Les troubles du rythme qui débute après les premières années de vie ont plus de risque de durer dans le temps.
-
Quelle prise en charge proposer ?
La prise en charge de trouble du rythme de l’enfant, dépend de l’âge de l’enfant, de la nature du trouble du rythme et des conséquences fonctionnelles de celui-ci.
Chez l’enfant de moins de 1 an, ne décrivant pas ses symptômes, et dont le risque de récidive de TSV par réentrée sur une voie accessoire est de 50%, le consensus est de proposer un traitement antiarythmique préventif. Les molécules les plus utilisées à cet âge sont les bétabloquants, l’amiodarone et la flécaïnide pour certaines équipes. La prescription sera fonction du poids de l’enfant. Il est alors nécessaire de faire des préparations en pharmacie et d’adapter régulièrement la posologie à la prise de poids. Le traitement est proposé pour une durée de 6 à 12 mois qui couvre la période la plus à risque de récidive. Passé cette période, le traitement peut-être interrompu. La prise en charge consiste alors, principalement, en l’éducation thérapeutique des parents afin que ceux-ci puissent dépister une éventuelle récidive.
La réduction du flutter néonatal peut être obtenue par cardioversion électrique ou médicamenteuse, ou encore par stimulation atrial (essentiellement par voie œsophagienne chez le nouveau-né), sans nécessité de traitement au long court si l’enfant n’a pas de cardiopathie associée.
Pour les TSV de l’enfant plus grand, qui décrit des accès des tachycardies bien toléré sur le plan hémodynamique, la prise en charge peut se résumer à l’enseignement des manœuvres vagales lorsque que les crises ne sont pas trop fréquentes. Les manœuvres vagales réalisables par un enfant ou un adolescent sont : la manœuvre de Valsalva, le fait d’expirer contre un obstacle, l’ingestion d’un grand verre d’eau glacé ou encore le fait de se mettre en position du poirier. Si ces techniques ne sont pas efficaces, on peut proposer de prescrire un « traitement minute » qui consiste à prendre, en automédication, un comprimé de bétabloquant ou d’un autre anti arythmique afin de faire cesser la crise. En cas de crises de tachycardie très fréquentes et handicapantes, le traitement antiarythmique peut être pris de façon préventive, quotidienne, en attendant soit une régression spontanée soit un traitement définitif par ablation.
-
L’ablation endocavitaire est-elle possible chez l'enfant et à quel âge ?
L’ablation endocavitaire est techniquement possible à tout âge. Des cas d’ablations chez des nouveaux nés de moins de 2 kg ont même été rapportés dans la littérature. Cependant les indications d’ablation chez les petits enfants sont tout à fait exceptionnelles et uniquement retenues en cas d’échec du traitement médical d’une tachycardie mettant en jeu le pronostic vital ou lorsque le contrôle de la tachycardie se fait au prix d’effets secondaires graves du traitement antiarythmique. En effet le rapport bénéfice/risque n’est pas en faveur de l’ablation chez le petit enfant car l’évolution spontanée est souvent favorable et le risque de complications de l’ablation plus important que chez le grand enfant ou l’adulte. La définition du « petit enfant » varie selon les sociétés savantes, la société européenne de cardiologie a retenu l’âge de 5 ans comme étant la limite d’âge au-delà duquel le traitement définitif par ablation endocavitaire peut être envisagé en alternative à un traitement médicamenteux, pour la société nord-américaine de rythmologie, la limite est de 15kg.
Chez le petit enfant, les indications d’ablation concerne donc exclusivement les troubles du rythme mettant en jeu le pronostic vital ou les substrats qui ne seront plus accessibles par voie endocavitaire après une chirurgie cardiaque (palliation de ventricule unique par dérivation cavo-pulmonaire totale ou annuloplastie risquant d’exclure une voie accessoire). Chez l’enfant plus grand, l’ablation endocavitaire peut-être proposé en cas de tachycardie supra ventriculaire récidivante qu’elle soit maitriser ou non par le traitement médicamenteux.
En cas de syndrome de Wolff-Parkinson-White, l’exploration endocavitaire avec option d’ablation est indiquée, que l’enfant fasse des accès de tachycardie ou non, avant l’entrée au collègue. Cette exploration complète l’épreuve d’effort qui est rarement contributive, et renseigne sur la période réfractaire antérograde de la voie accessoire et le risque potentiel de mort subite par transmission d’une fibrillation atriale en fibrillation ventriculaire. Le risque de fibrillation atriale chez l’enfant est exceptionnel avant cet âge et c’est pourquoi la limite de 8-10 ans est retenue par la plupart des électrophysiologistes pédiatriques pour réaliser l’exploration. Au terme de l’exploration, la période réfractaire antérograde de la voie accessoire de base et sous Isuprel est renseignée, de même que sa localisation et l’inductibilité ou non de rythme réciproque. L’exploration peut-être alors complété par une ablation de la voie accessoire si la voie accessoire n’a pas une localisation à risque de complication, si elle est potentiellement dangereuse et/ou responsable de tachycardie. A l’opposé, une voie accessoire non dangereuse, dont la localisation est à risque ou qui n’est pas responsable d’accès de rythme réciproque sera respectée. En cas de voie accessoire « mal placée », potentiellement dangereuse et/ou responsable d’accès de tachycardie, l’ablation pourra être temporisée. Dans ce cas l’enfant est placé sous traitement par flécaïnide jusqu’à qu’il ait atteint un gabarit permettant d’envisager l’ablation et que les risque de celle-ci ait été expliqué et compris par le patient et sa famille.
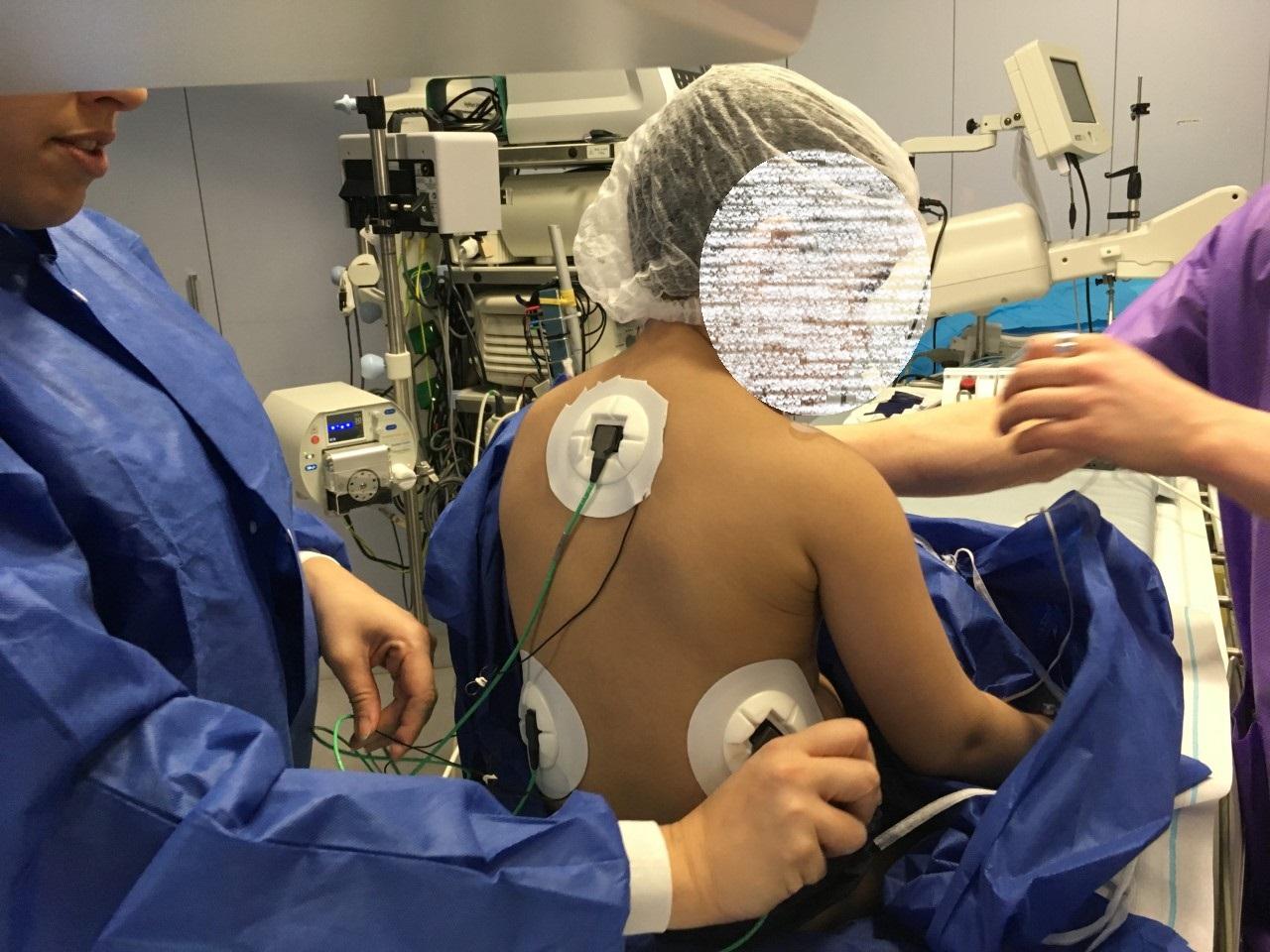
Image 1: Positionnement des patchs nécessaire à la cartographie électro-anatomique chez un enfant de 8 ans. La partie collante du patch peut éventuellement être découpée chez les enfants plus petits.
Les différents systèmes de cartographies sont largement utilisés chez l'enfant car ils permettent de diminuer l'exposition aux radiations ionisantes.
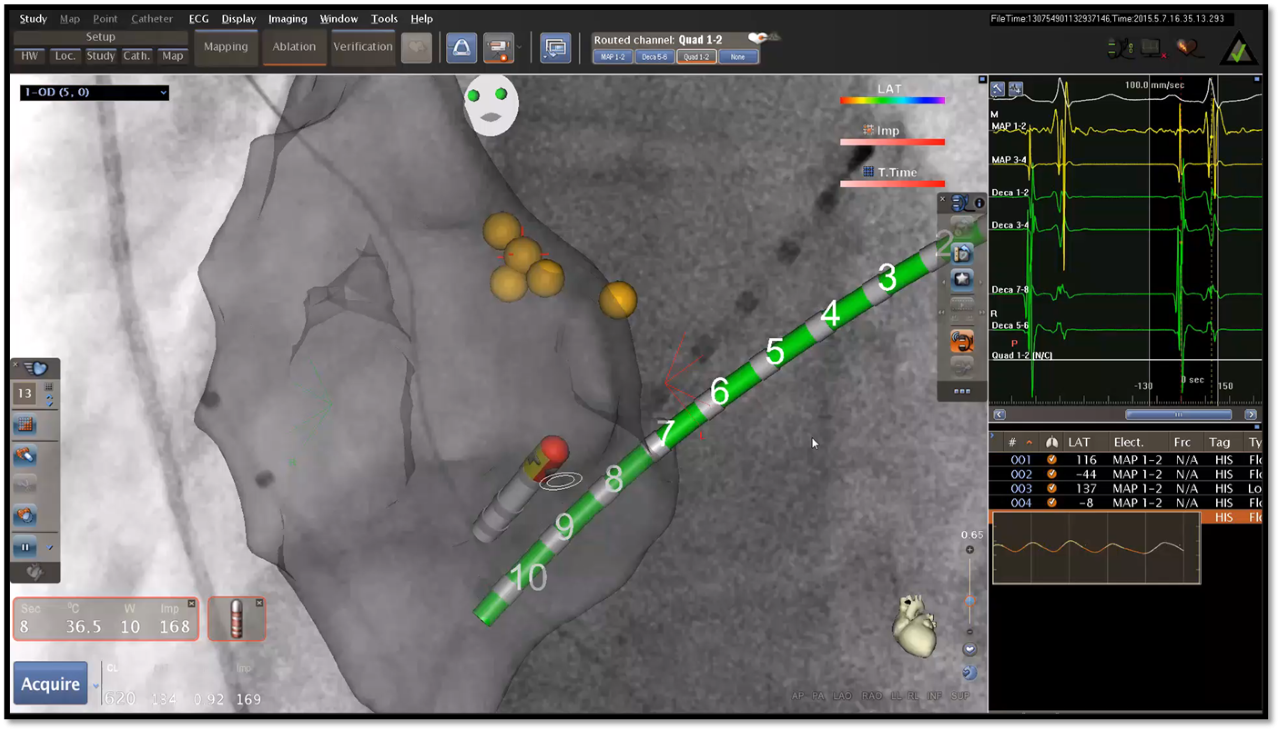
Image 2: Ablation d'une dualité nodale avec Carto 3D-UNIVU (chez un autre patient que image1).
-
L’enfant peut-il avoir un scolarité normale et faire des activités sportives avec une arythmie ?
En dehors des arythmies clairement déclenchées par les efforts de façon reproductible, le sport n’est pas contre-indiqué en cas de trouble du rythme supraventriculaire.
En cas de syndrome de Wolff Parkinson White, la pratique du sport de compétition est déconseillée à partir de l’âge de 8-10 ans ou temps que l’exploration électrophysiologique n’a pas été effectuée. En attendant que celle-ci soit réalisée, la pratique sportive de loisir peut être autorisée sous couvert d’une prescription de flecaïnide.
Pour l’école, la mise en place d’un Projet d’Accueil Individualisé (PAI) peut être nécessaire, notamment en cas de traitement minute à administrer sur le temps scolaire.
Vous devez être connecté pour poster un commentaire
