L'insuffisance cardiaque
Elodie Huet, infirmière en pratiques avancées, CHRU Nancy
Introduction
Il y a 10 ans, le « risque » de développer une insuffisance cardiaque au cours de sa vie était de 1 sur 5 (1).
Aujourd’hui, environ 2.3% de la population est atteinte de cette pathologie. Chez les sujets âgés de 70 ans et plus, ce chiffre avoisine même les 10% (2). Le vieillissement de la population ne laisse pas prédire une baisse de la population concernée dans les années à venir.
L’insuffisance cardiaque est une maladie grave. Le présage de décès dans la population insuffisante cardiaque est de 14%, allant jusque 25% dans les cas d’insuffisance cardiaque aigue. La pathologie représente à elle seule la moitié des séjours potentiellement évitables, soit plus de 156 000 hospitalisations pour l’année 2015 et 160 000 pour 2017 (3). Concernant le suivi de ces patients, un rapport sur les charges et produits de l’assurance maladie en concordance avec le plan « Ma santé 2022 », a mis en évidence que 31% des patients hospitalisés ont été réhospitalisés l’année suivante, dont 15.5% dans les 3 mois suivant leur retour à domicile.
Nous avons, en qualité de soignant, un rôle important à jouer dans le dépistage de la maladie, l’autonomisation des patients, à travers un transfert de nos connaissances et l’assurance d’un suivi observé afin de leur permettre le maintien d’une qualité de vie satisfaisante et une prise en charge qui se voudrait majoritairement ambulatoire.
I. Physiopathologie de l’insuffisance cardiaque
L’insuffisance cardiaque (IC) traduit une faiblesse du muscle cardiaque (myocarde). En raison d’anomalies physiopathologiques, le cœur n’est plus en capacité de fournir un débit sanguin suffisant pour répondre aux besoins en oxygène du métabolisme à l’effort et/ou au repos. Cet état résulte d’une altération de remplissage et/ou d’éjection du ventricule gauche (VG).
Dans un premier temps, un remodelage ventriculaire physiologique va compenser cette défaillance, visant à accroître la capacité du ventricule et ainsi maintenir un Volume d’Ejection Systolique (VES) satisfaisant ; c’est-à-dire un volume sanguin éjecté par le VG à chaque systole proche de la capacité initiale (Loi de Laplace). Cette « transformation » physiologique (hypertrophie et/ou dilatation) a ses limites (Figure 1). Si ce remodelage est un temps bénéfique dans la compensation de cette défaillance cardiaque, il devient délétère à moyen et long terme. S’en suit alors une décompensation avec l’apparition de symptômes cliniques (4).
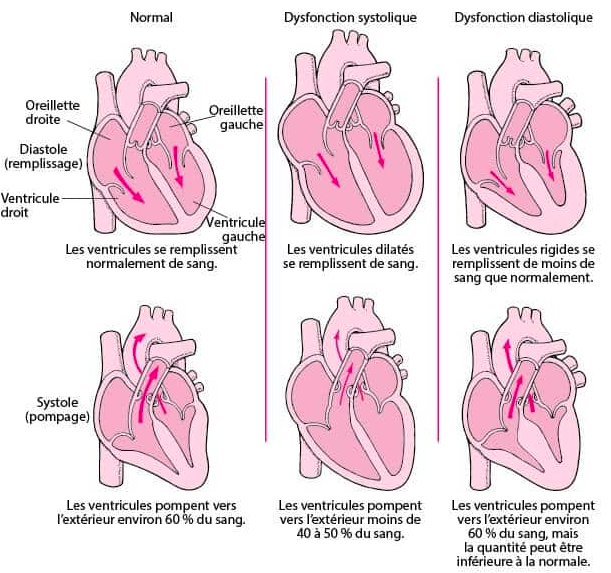
Figure 1 : Insuffisance cardiaque : Anomalies du pompage et du remplissage (Source msdmanuals.com)
L’IC peut prendre différentes formes :
- Systolique, lorsqu’il s’agit d’un défaut d’éjection, de vidange des ventricules.
- Diastolique, lorsqu’il s’agit d’une anomalie de remplissage des ventricules. Dans ce cas, Il n’y a pas d’anomalie de la contraction, l’éjection du sang par les ventricules est normale, on parle d’insuffisance cardiaque à Fraction d’Ejection (FE) « préservée » ou « conservée ».
- Droite, lorsqu’elle concerne le ventricule droit. Entrainant une élévation des pressions veineuses pulmonaires.
- Gauche, lorsqu’elle concerne le ventricule gauche. Entrainant une élévation des pressions veineuses systémiques.
- Globale, lorsque des signes d’Insuffisance Cardiaque Droite (ICD) apparaissent au cours d’une Insuffisance Cardiaque Gauche (ICG).
Selon l’importance des symptômes et leur retentissement sur le métabolisme en général, on qualifie l’IC de légère, modérée ou sévère (5).
Quand cet état apparaît brutalement ou est récent, on parle d’IC « aiguë » ou « de novo ». En cas de récidive d’épisode(s) de décompensation(s) on parle d’IC chronique.
La symptomatologie est définie par le retentissement de l’altération du ventricule sur sa pré et post charge. Les symptômes fonctionnels ressentis par le patient présentant une ICG sont dominés par une dyspnée d’effort voire de repos ou de décubitus (orthopnée). Dans un contexte d’ICD, les signes cliniques sont majoritairement en lien avec le territoire cave inférieur, du fait de l’élévation de la pression dans l’auricule droit et de la pesanteur. On retrouve très facilement chez ces patients, des œdèmes périphériques (notamment des membres inférieurs), une prise pondérale et parfois une hépatomégalie ou une turgescence jugulaire (figure 2).
|
Insuffisance cardiaque Gauche
|
Insuffisance cardiaque Droite |
|
|
|
Figure 2 : Signes cliniques et symptôme de l’insuffisance cardiaque
L’IC est un syndrome qui fait suite à une atteinte structurelle (muscle / valve) ou fonctionnelle sous-jacente. Les étiologies à son origine sont multiples : ischémie voire nécrose myocardique, valvulopathie, cardiopathie d’origine rythmique (fibrillation atriale, troubles du rythme d’origine ventriculaire) ou hypertensive, toxicité médicamenteuse ou radio-induite, carence martiale ou vitaminique, pathologie de surcharge (amylose, maladie de Fabry, hémochromatose, …), cardiopathie d’origine génétique. Il est ainsi nécessaire de toujours rechercher la cause d’une IC afin de la traiter dans sa globalité. En fonction du retentissement physiologique, on parlera :
- Cardiopathies restrictives, lorsque les parois des ventricules se rigidifient (avec ou sans épaississement). Les parois ventriculaires non compliantes altèrent alors le remplissage ventriculaire en diastole.
- Cardiopathies dilatées, lorsque le(s) ventricules(s) affaibli(s) se dilatent réduisant la force de contraction du myocarde et par conséquent l’éjection du sang en systole.
- Cardiopathies hypertrophiques, lorsqu’un épaississement excessif du VG (majoritairement du septum) entraîne une non compliance, réduisant l’éjection du sang contenu par celui-ci en systole.
Il est primordial de dépister et de prendre en charge les facteurs de risques favorisant le développement des cardiopathies précédemment citées : tabagisme, dyslipidémie, surcharge pondérale, athérosclérose, hypertension artérielle, diabète, syndrome d’apnée du sommeil… (5).
Les retentissements ou la cause de l’IC peuvent être multi-organiques, voire provenir d’une atteinte neuro-hormonale (système adrénergique, rénine-angiotensine, aldostérone) (4).
L’ensemble de ces éléments permet d’appréhender la complexité qu’est le traitement de l’insuffisance cardiaque et sa prise en charge. Préalablement à cette prise en charge et à l’instauration d’un traitement adapté, il convient de poser le diagnostic d’insuffisance cardiaque et d’en rechercher la ou les étiologie(s) pour prévenir son évolution de manière optimale.
II. Diagnostic et pronostic
L’IC est à ses débuts une maladie « sournoise » et insidieuse. Certains patients asymptomatiques dans un premier temps présentent tout de même une/des anomalie(s) cardiaque(s) structurale(s) et/ou fonctionnelle(s). Puis apparaissent des symptômes et signes cliniques. Le diagnostic doit être le plus précoce possible pour anticiper, prévenir l’évolution vers un stade avancé de l’insuffisance cardiaque. Les recommandations Européennes de 2016 préconisent de rechercher de manière systématique une insuffisance cardiaque débutante chez les sujets à risque. Cela passe par une analyse approfondie des antécédents (rythmique, ischémique, hypertensive, valvulaire, congénitale, toxique, rénaux, endocrinien…), des symptômes du patient (orthopnée, dyspnée, asthénie, prise de poids), des éléments cliniques (œdèmes, turgescence jugulaire, crépitants, bruits du cœur anormaux (galop, souffle)) et paracliniques en faveur d’une cardiopathie sous-jacente inconnue qui pourrait être à l’origine d’une dysfonction structurelle ou fonctionnelle.
Les comorbidités telles que la carence martiale (6), l’apnée du sommeil (7), les pathologies rénales chroniques, les états infectieux ou la dénutrition ne doivent pas être négligés. (8).
Si l’anamnèse réalisée se révèle positive, un dosage des BNP (Brain Natriuretic Peptide) et NT-pro BNP (fragment N-terminal du pro Brain Natriuretic Peptide) est préconisé en première intention. Leur libération par les cardiomyocytes signe une élévation de la pression sanguine sur les parois des cavités cardiaques, notamment des ventricules, et un étirement des fibres myocardiques. Elle permet également l’inhibition du système rénine angiotensine aldostérone et de ce fait une vasodilatation permettant de réduire les résistances systémiques et la surcharge hydrosodée induite par l’insuffisance cardiaque (9).
Ces marqueurs ne sont pas spécifiques de la fonction cardiaque, leur concentration est très variable selon l’âge, la corpulence, le sexe et certaines pathologies tels que l’insuffisance rénale, les dysthyroïdies, l’insuffisance surrénalienne… Il est donc préférable, car complémentaire, d’associer systématiquement l’échocardiographie transthoracique (ETT) au dosage des NT-pro BNP et BNP pour le diagnostic de l’insuffisance cardiaque. Ces marqueurs ont également une valeur pronostique dans la prise en charge des patients présentant une IC chronique (10) (Figure 3).
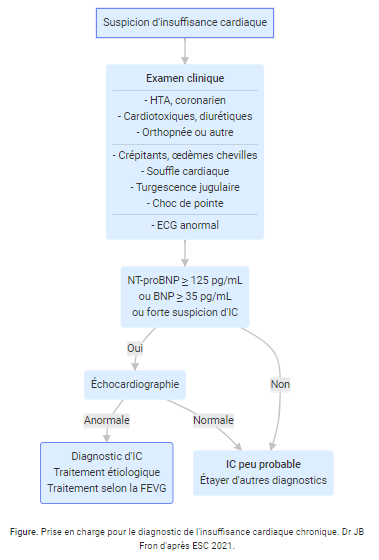
Figure 3 : Prise en charge pour le diagnostic de l'insuffisance cardiaque chronique. Dr JB Fron d'après ESC 2021.
L’ETT permet notamment d’évaluer la fonction systolique du VG et de calculer la Fraction d’Ejection du VG (FEVG), qui permet de classifier l’insuffisance cardiaque selon les 3 catégories suivantes:
- Insuffisance cardiaque à fraction d’éjection préservée (FEVG >50%)
- Insuffisance cardiaque à fraction d’éjection modérément diminuée (FEVG <50% mais >40%)
- Insuffisance cardiaque à fraction d’éjection altérée (FEVG <40%)
Elle tient également un rôle primordial dans le cadre du bilan étiologique et du retentissement de l’IC.
L’évaluation du degré de dilatation et de compliance de la veine cave inférieure, ainsi que la quantification indirecte de la pression artérielle pulmonaire (PAPs), permettent de monitorer le patient sur le plan volémique et d’aider à équilibrer les traitements de fond à visée symptomatique. La congestion pulmonaire par l’intermédiaire de l’échographie pulmonaire, est quant à elle, un excellent moyen prédictif du risque de décompensation de la maladie (11).
Le retentissement fonctionnel et le pronostic des patients sont en lien direct avec la FEVG et l’état congestif. L’objectif est ainsi d’optimiser la prise en charge thérapeutique de telle sorte que la fonction cardiaque soit la moins altérée possible et le patient en euvolémie.
L’évaluation de la fragilité du patient et sa prise en compte dans l’accompagnement thérapeutique a également tout son sens quant à la limitation de l’évolution de la maladie et la perte de qualité de vie qui en dépend (12).
L’insuffisance cardiaque est une maladie chronique complexe, résultant fréquemment de l’imbrication de plusieurs pathologies, elles-mêmes chroniques pour la plupart. L’utilisation du « score MAGGIC » (13) (14) permet d’attirer l’attention sur le pronostic de la maladie en fonction des signes cliniques, biologiques, des symptômes, des facteurs de risque et comorbidités du patient.
III. Thérapeutique
Le traitement de l’insuffisance cardiaque repose autant sur l’introduction d’un traitement pharmacologique que sur le respect de mesures hygiéno-diététique par le patient (Recommandation de classe I-A / Société Européenne de Cardiologie).
Le traitement est fonction de la FEVG, de la symptomatologie, de la fonction rénale et prend en considération des marqueurs ioniques tel que la kaliémie et la natrémie.
Doivent ainsi être introduit et titrés jusqu’à la dose maximale toléré par le patient (Figure 4) :
- Inhibiteur de l’enzyme de conversion (IEC) ou Inhibiteur des récepteurs de l’angiotensine et de la néprilysine (ARNI) ou Antagoniste des récepteurs de l’angiotensine II (ARAII)
- Bétabloquants (BB)
- Antagonistes des récepteurs aux minéralo-corticoïdes (ARM) appelés également anti aldostérone
- Inhibiteurs du co-transporteur 2 sodium-glucose (SGLT2 / gliflozines)
En cas de congestion, un diurétique de l’anse (majoritairement) pourra se voir ajouter au traitement de fond précédemment décris.
Une couverture vaccinale efficiente contre la grippe et pneumoccoque est vivement recommandé.
|
Classe pharmacologique |
Mécanisme d’action |
Principaux effets secondaires |
|
IEC / ARAII |
Bloque les récepteurs de l’angiotensine II (vasoconstrictrice) -> diminution de la production d’aldostérone -> vasodilatation -> soulage le travail du cœur
|
Angioœdème, toux Hyperkaliémie Altération de la fonction rénale
|
|
BB |
Ralentit le rythme cardiaque, réduit les besoins en O2 -> soulage le travail du cœur, action de remodelage
|
Etourdissements, faiblesse, fatigue, cauchemars, dysfonction érectile Sujet diabétique : diminution de la perception des hypoglycémies
|
|
ARM |
Bloque l’action de l’aldostérone, aide à limiter la rétention hydrique, complète l’action du diurétique
|
Hyperkaliémie, sécheresse buccale, sensation vertigineuse, douleurs gastrique
|
|
SGLT2 |
Favorise la réabsorption du glucose au niveau rénale -> augmentation de la diurèse |
Infections uro-génitales, hypotension, déshydratation Altération de la fonction rénale
|
|
Diurétiques de l’Anse |
Stimule l’excrétion rénale du sodium et de l’eau -> diminution du volume sanguin -> diminution TA -> soulage le travail du cœur
|
Déshydratation, hypokaliémie, hyponatrémie, hypovolémie, hypotension orthostatique
|
|
Figure 4 : Traitement pharmacologique de l’insuffisance cardiaque, mécanisme d’action et principaux effets secondaires |
En parallèle de l’observance aux traitements pharmacologiques, le patient se doit adopter une hygiène de vie saine et rigoureuse.
Deux « acronymes » doivent être connus de nos patients :
EPON : les 4 règles de vie à s’efforcer de respecter
- Exercice physique : Faire de l’exercice physique, d’endurance adaptée de manière quotidienne (30min/j) ou 20minutes trois fois par semaine minimum d’activité physique endurante générant un essoufflement léger à modéré.
- Prendre son Poids régulièrement sur la même balance dans les mêmes conditions
- Observance : prendre son traitement sans discontinuité et respecter son calendrier de consultations de suivi
- Ne pas saler : avoir une alimentation hyposodée et non sans sel strict pour éviter la rétention d’eau et de sel
Ne pas trop boire :1l250 à 1l500 d’apports hydriques quotidien (tout apport confondu), à moduler en cas de forte chaleur et à adapter selon la spécificité de l’insuffisance cardiaque pour chaque patient.
EPOF : les symptômes à évaluer régulièrement pour repérer rapidement une aggravation et prévenir une décompensation qui pourrait nécessiter une hospitalisation
- Essoufflement : apparition et/ou aggravation de la dyspnée, apparition d’une orthopnée
- Poids : prise de poids supérieure ou égale à 2kgs en 3jours / perte de poids trop rapide associée ou non à une soif et/ou une sécheresse buccale
- Œdèmes : apparitions ou aggravation d’œdèmes (essentiellement des membres inférieurs)
- Fatigue : fatigue plus soutenue que d’habitude et dont le repos n’est pas compensateur
La compréhension de la maladie et de ses possibles répercussions par les patients, permet de les autonomiser dans la gestion de leur IC. Ceci par l’intermédiaire de parcours d’éducation thérapeutique structurés comprenant des interventions pluri professionnelles.
En complément des acronymes EPOF et EPON, d’autres thématiques doivent-être abordées avec les patients car elles s’intègrent dans la globalité de sa prise en charge. Pour certaines, il s’agit de transmettre un savoir, pour d’autre de dépister des fragilités ou comorbidités et permettre une prise en charge parallèle spécifique.
- Les troubles du sommeil (apnée du sommeil)
- L’absence d’automédication, notamment les comprimés effervescents en vente libre (riche en sodium) et la prise d’anti-inflammatoire non stéroïdien (AINS).
- Ne pas compenser le sel de table par du sel à base de chlorure de potassium (Le potassium en excès étant tout aussi délétère pour l’organisme – responsable d’arythmie parfois létale)
- Ne pas craindre les questions autour de la sexualité des patients mais y répondre en les accompagnant au mieux ou les orientant vers une prise en charge spécifique (sexologue).
- Aborder de possibles difficultés psychosociales
De manière plus individuelle, sensibiliser les patients à consulter rapidement en cas d’apparition d’une toux sèche, à la prise du pouls pour alerter en cas d’irrégularité et de fréquence cardiaque inférieure à 45 battements par minutes.
Pour les situations les plus avancées, il peut être discuté l’implantation d’un défibrillateur lorsqu’il s’agit d’IC chronique avec persistance d’une FEVG ≤ 35%. Ceci en prévention d’une mort subite par fibrillation ventriculaire, chez des patients a autonomie préservé et pronostic vital satisfaisant à moyen terme.
Les patients les plus sévères se voient orientés et pris en charge par des équipes d’insuffisance cardiaque sévère en vue d’une éventuelle assistance ventriculaire ou une greffe cardiaque selon les situations de vie.
Conclusion
L’insuffisance cardiaque est une pathologie aux multiples étiologies. Elle est complexe et son pronostic dépends de la précocité du dépistage et de sa prise en charge. L’atteinte du myocarde régresse dans de rare cas, mais la mise en place d’un traitement adapter et d’une hygiène de vie rigoureuse permettent de la stabiliser. Cette stabilité clinique se répercute sur le maintien de la qualité de vie des patients et n’est possible qu’à travers une relation de confiance entre le patients et les multiples acteurs professionnels qui constituent son parcours de soin (cardiologue, médecin généraliste, pharmacien, biologiste, kinésithérapeute, diététicien, infirmier en secteur de soins ou libéral, IPA, infirmier avec protocole de coopération IC ou échocardiographique, infirmier d’éducation thérapeutique…)
Bibliographie
1. Bui AL, Horwich TB, Fonarow GC. Epidemiology and risk profile of heart failure. Nat Rev Cardiol. 2011;8(1):30‑41.
2. Insuffisance cardiaque [Internet]. Santé Publique France. Disponible sur: https://www.santepubliquefrance.fr/maladies-et-traumatismes/maladies-cardiovasculaires-etaccident-vasculaire-cerebral/insuffisance-cardiaque
3. La lutte contre les réhospitalisations, priorité pour améliorer la pertinence du parcours insuffisance cardiaque (Cnam) [Internet]. Disponible sur: https://www.cardioonline.fr/Actualites/Depeches/lutte-contre-rehospitalisations-priorite-pour-ameliorerpertinence-parcours-insuffisance-cardiaque
4. Juillière Y. Physiopathologie de l’insuffisance cardiaque. Soins. 2013;58(774):26‑8.
5. Delahaye F, Harbaoui B, Cart-Régal V, De Gevigney G. Épidémiologie et physiopathologie de l’insuffisance cardiaque chronique. soins. 2008;53(730):36‑9.
6. Grote Beverborg N, van Veldhuisen DJ, van der Meer P. Anemia in Heart Failure: Still Relevant? JACC Heart Fail. mars 2018;6(3):201‑8.
7. Javaheri S, Barbe F, Campos-Rodriguez F, Dempsey JA, Khayat R, Javaheri S, et al. Sleep Apnea: Types, Mechanisms, and Clinical Cardiovascular Consequences. J Am Coll Cardiol. 2017;69(7):841‑58.
8. Bozkurt Biykem, Aguilar David, Deswal Anita, Dunbar Sandra B., Francis Gary S., Horwich Tamara, et al. Contributory Risk and Management of Comorbidities of Hypertension, Obesity, Diabetes Mellitus, Hyperlipidemia, and Metabolic Syndrome in Chronic Heart Failure: A Scientific Statement From the American Heart Association. Circulation. 2016;134(23):535‑78.
9. Collin-Chavagnac D. Facteur natriurétique de type B ( brain natriuretic peptide [BNP]). Biologie médicale. 2014;9(3):1‑6
10. Logeart D, Thabut G, Jourdain P, Chavelas C, Beyne P, Beauvais F, et al. Predischarge B-type natriuretic peptide assay for identifying patients at high risk of re-admission after decompensated heart failure. Journal of the American College of Cardiology. 2004;43(4):635‑41.
11. Miglioranza MH, Picano E, Badano LP, Sant’Anna R, Rover M, Zaffaroni F, et al. Pulmonary congestion evaluated by lung ultrasound predicts decompensation in heart failure outpatients. Int J Cardiol. 1 août 2017;240:271‑8.
12. Gastelurrutia P, Lupón J, Altimir S, de Antonio M, González B, Cabanes R, et al. Fragility is a key determinant of survival in heart failure patients. Int J Cardiol. 15 juill 2014;175(1):62‑6
13. Khanam SS, Choi E, Son J-W, Lee J-W, Youn YJ, Yoon J, et al. Validation of the MAGGIC (MetaAnalysis Global Group in Chronic Heart Failure) heart failure risk score and the effect of adding natriuretic peptide for predicting mortality after discharge in hospitalized patients with heart failure. PLoS One. 2018;13(11):e0206380.
14. Rich JD, Burns J, Freed BH, Maurer MS, Burkhoff D, Shah SJ. Meta-Analysis Global Group in Chronic (MAGGIC) Heart Failure Risk Score: Validation of a Simple Tool for the Prediction of Morbidity and Mortality in Heart Failure With Preserved Ejection Fraction. J Am Heart Assoc. 16 oct 2018;7(20):e009594
Vous devez être connecté pour poster un commentaire
