Défibrillateurs cardiaques automatiques implantables
Dr Pierre Baudinaud, Hôpital Européen Georges Pompidou, Paris
Mai 2022
Introduction
L’implantation d’un défibrillateur automatique implantable (DAI) occupe aujourd’hui une place importante dans l’arsenal thérapeutique de la cardiologie moderne. Le nombre d’implantations croît d’années en années. Initialement évalués dans la prévention secondaire de la mort subite, leur efficacité a été prouvée en prévention primaire chez les patients à haut risque rythmique en réduisant grandement la mortalité liée aux arythmies ventriculaires (Tableau 1).
Leur principal rôle est d’analyser le rythme cardiaque de façon continue et de traiter si nécessaire les arythmies ventriculaires détectées. Dans certains cas, ils ont aussi une fonction de stimulation.
Les indications d’implantations ainsi que le suivi de ces patients sont encadrées par des recommandations internationales précises.
Après un bref rappel de sa composition et de ses principes de fonctionnement, nous détaillerons les indications, les complications propres à leur implantation ainsi que le suivi des patients.
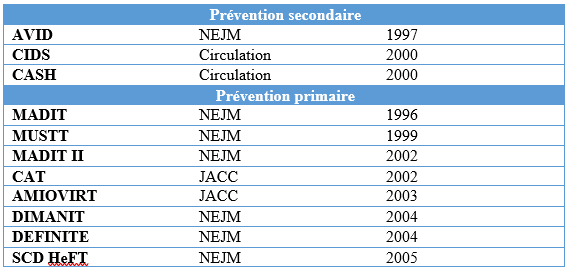
Tableau 1. Principaux essais ayant évalué l'intérêt de l'implantation d'un défibrillateur
Composition d’un défibrillateur
Il existe à l’heure actuelle deux types de défibrillateurs. Les défibrillateurs endocavitaires avec des sondes intra cardiaques et les défibrillateurs sous cutanés sans sonde intra cardiaque. Ces deux types d’appareil sont composés d’un boitier et d’au moins une sonde. Contrairement aux défibrillateurs endocavitaires, le défibrillateur sous cutané ne peut réaliser de stimulation anti bradycardique ou d’ATP (Anti Tachycardia Pacing).
Le boitier
Il est composé d’une coque étanche en titane avec à son pôle supérieur les connecteurs entourés d’une coque généralement en polymère (Figure1). Il contient la batterie, les condensateurs, l’antenne de télémétrie ainsi que les circuits électroniques.
La batterie
Les défibrillateurs endocavitaires ont deux circuits électriques, un à basse énergie permettant d’assurer la fonction de stimulation et un à haute énergie permettant de délivrer les chocs électriques. Les piles lithium-iode des stimulateurs cardiaques sont insuffisantes pour la défibrillation ainsi la batterie des défibrillateurs est une pile lithium-oxyde de vanadium et argent.
Les condensateurs
Ils permettent de stocker une charge électrique et sont indispensables pour délivrer le choc. Ils sont reformatés automatiquement de façon régulière afin de régénérer la couche diélectrique à leurs surfaces et de minimiser l’usure prématurée.
Les circuits électroniques
Permettent la détection et parfois la stimulation. Ils contiennent les algorithmes de stimulation, de détection ainsi que les algorithmes de discrimination.
Les sondes
Plus complexes et plus fragiles que les sondes de stimulateurs cardiaques, elles représentent le maillon faible des défibrillateurs (1). Elles sont responsables de la majeure partie des complications.
Elles sont constituées d’un isolant externe ainsi que d’isolants internes composés de silicone, polyuréthane et/ou de résines fluorocarbonnées. Au sein des isolants se trouvent les conducteurs pour le circuit de stimulation / détection et de défibrillation.
-
Pour les défibrillateurs endocavitaires
A leur extrémité distale nous retrouvons une visse, deux électrodes de stimulation / détection (parfois une seule électrode : BOSTON) ainsi qu’une à deux électrodes de défibrillation appelées coïls. Ces coïls ont la capacité d’accumuler une importante charge électrique rendant possible la défibrillation.
A leur extrémité proximale est située le connecteur. Il est unique pour les sondes DF4 et multiple (2 à 3 extrémités) pour les sondes DF1.
-
Pour les défibrillateurs sous cutanée
La sonde est constituée d’un coïl entouré par deux électrodes de détection. (Figure 2)

Figure 1 : Boitier d'un défibrillateur simple chambre endocavitaire
 Figure 2 : Boitier et sonde d'un défibrillateur sous cutané.
Figure 2 : Boitier et sonde d'un défibrillateur sous cutané.
Principes de fonctionnement d’un défibrillateur
Les fonctions anti bradycardiques ne seront pas abordées au cours de ce chapitre. Elles sont identiques à celles des stimulateurs cardiaques et ne sont présentes que pour les défibrillateurs endocavitaires.
Les fonctions propres d’un défibrillateur sont la détection et la discrimination des arythmies ventriculaires ainsi que le traitement de ces dernières.
Détection et discrimination des arythmies ventriculaires
La détection d’une arythmie ventriculaire débute lorsque la fréquence ventriculaire s’élève au-dessus d’une fréquence programmée pendant un certain nombre de battements ou pour une durée déterminée. Puis les algorithmes de discrimination entrent en jeu afin d’établir s’il s’agit d’une tachycardie supra ventriculaire rapidement conduite aux ventricules ou s’il s’agit bel et bien d’un trouble du rythme ventriculaire.
Zones de détection
Il est d’usage de programmer plusieurs zones de détection. Généralement au moins une zone de tachycardie ventriculaire et une zone de fibrillation ventriculaire. Les recommandations concernant les zones de détection et les durées de détection diffèrent entre les différents constructeurs et selon l’indication de l’implantation(2). Il faut retenir que les zones doivent être assez hautes et les durées de détection assez longues pour éviter des chocs inappropriés et/ou inutiles (3).
Pour une implantation pour la prévention primaire:
- Zone de tachycardie ventriculaire entre >180 /min ; 30 à 40 cycles ou 6 à 12 secondes
- Zone de fibrillation ventriculaire > 230-250/min ; 20 à 30 cycles ou 5 secondes.
- Parfois une deuxième zone de détection peut être programmée afin de monitorer ou même de traiter d’éventuelles arythmies ventriculaires lentes.Pour une implantation pour la prévention secondaire
- Zone de tachycardie ventriculaire : fréquence de la tachycardie – 10 à 20/min
- Zone de fibrillation ventriculaire : identique qu’en prévention primaire
Pour les défibrillateurs sous cutanés
- Une zone de choc conditionnel entre 220 et 250/min
- Une zone de choc > 250/min
Discrimination
Étape cruciale avant un éventuel traitement d’une tachycardie ventriculaire. Elle permet d’éviter une thérapie inappropriée.
La discrimination rentre en jeu seulement dans les zones de détection de tachycardies ventriculaires. Concernant les zones de fibrillation ventriculaire seule la fréquence ventriculaire rentre en jeu, il n’y a pas de discrimination.
La discrimination est basée sur des algorithmes plus ou moins complexes. Elle doit avoir la meilleure sensibilité afin de ne pas passer à côté d’une tachycardie ventriculaire mais doit être la plus spécifique possible afin d’éviter les thérapies inappropriées.
- Discrimination pour les défibrillateurs simple chambre:
Les algorithmes associent le début brutal, la stabilité de la tachycardie avec plus ou moins la morphologie de l’EGM.
- Discrimination pour les défibrillateurs double ou triple chambre
Les algorithmes de ces défibrillateurs reprennent ceux des défibrillateurs simple chambre en prenant en considération la relation oreillettes / ventricule.
- Discrimination des défibrillateurs sous cutanés
Principalement basée sur la morphologie du signal.
Traitement des arythmies ventriculaires
Une fois la détection et la discrimination réalisées, le défibrillateur traite l’arythmie. Pour cela deux possibilités soit par la réalisation d’un ATP (Antitachycardia Pacing) soit par la réalisation d’un choc électrique interne. Pour rappel, les défibrillateurs sous cutanés ne peuvent pas réaliser d’ATP.
- ATP : Antitachycardia Pacing
Le principe de l’ATP est de stimuler plus rapidement que la tachycardie ventriculaire afin de capturer le circuit de tachycardie et d’arrêter la tachycardie (overdrive). Elle est possible pour les arythmies organisées (tachycardies ventriculaires). Il en existe deux types : les bursts qui correspondent à une stimulation à fréquence fixe et les rampes qui correspondent à une stimulation à fréquence croissante.
Il est recommandé de programmer des ATP pour toutes les zones de thérapies y compris en zone FV. En effet, il a été prouvé que la réalisation d’ATP était efficace pour les tachycardies ventriculaires rapides permettant d’éviter des chocs et d’avoir de meilleurs résultats en terme de qualité de vie (4).
- Choc électrique interne
Il survient après réalisation d’un ATP. Il est toujours biphasique, son énergie et son vecteur son programmable.
Indications d’implantation des défibrillateurs
Les indications d’implantations découlent des études randomisées de la fin des années 90 début des années 2000. Les recommandations d’implantation sont fonction du type de prévention ainsi que de la cardiopathie sous-jacente (5;6). Ci-dessous, les indications les plus fréquentes.
Prévention secondaire
|
Recommandations |
Classe |
Niveau |
|
L’implantation d’un DAI est recommandée chez les patients avec de la FV documentée ou une TV mal tolérée hémodynamiquement en l’absence de cause réversible, à plus de 48 heures d’un infarctus et recevant un traitement chronique optimal ayant une espérance de vie ≥ 1 an avec un bon statut fonctionnel. |
I |
A |
|
L’implantation d’un DAI devrait être considérée chez les patients présentant des TV récurrentes (pas dans les 48 heures d’un infarctus) recevant un traitement chronique optimal ayant une FEVG normale ayant une espérance de vie ≥ 1 an avec un bon statut fonctionnel. |
IIa |
C |
DAI : Défibrillateur Automatique Implantable ; FV : Fibrillation Ventriculaire ; TV : Tachycardie ventriculaire
Prévention primaire
|
Recommandations |
Classe |
Niveau |
|
L’implantation d’un DAI est recommandée afin de réduire le risque de mort subite et la mortalité toute cause chez les patients IC symptomatiques (NYHA II-III) porteurs d’une cardiopathie ischémique (sauf si IDM dans les 40 jours) avec une FEVG ≤35% malgré un traitement médical optimal durant ≥ 3 mois et ayant une espérance de vie ≥ 1 an avec un bon statut fonctionnel. |
I |
A |
|
L’implantation d’un DAI devrait être considérée afin de réduire le risque de mort subite et la mortalité toute cause chez les patients IC symptomatiques (NYHA II-III) porteurs d’une cardiopathie non ischémique avec une FEVG ≤35% malgré un traitement médical optimal durant ≥ 3 mois et ayant une espérance de vie ≥ 1 an avec un bon statut fonctionnel. |
IIa |
B |
DAI : Défibrillateur Automatique Implantable ; Patients IC : Patients insuffisants cardiaque
Défibrillateur sous cutané
|
Recommandations |
Classe |
Niveau |
|
Le défibrillateur sous cutané devrait être considéré comme une alternative aux DAI chez les patients ayant une indication à un DAI lorsque la stimulation, la resynchronisation et les ATP ne sont pas nécessaires |
IIa |
C |
|
Le défibrillateur sous cutané devrait être considéré comme une alternative utile aux DAI endocavitaire lorsque l’accès veineux est difficile, après le retrait d’un DAI endocavitaire ou chez les jeunes patients avec un besoin long de thérapie par DAI. |
IIb |
C |
DAI : Défibrillateur Automatique Implantable
La procédure d’implantation (voire également fiches techniques)
Implantation d’un défibrillateur endocavitaire
Pour les défibrillateurs endocavitaires elle est similaire à la procédure d’implantation d’un stimulateur cardiaque bien détaillée dans le chapitre traitant de la stimulation cardiaque.
Il faut néanmoins s’assurer d’une bonne détection ventriculaire au moins supérieure ou égale à 5mV en per opératoire. En effet, une bonne détection à l’implantation permet de réduire le risque de sous détection lors des épisodes de fibrillation ventriculaire généralement microvoltés.
Il n’est plus recommandé actuellement de tester les défibrillateurs en post implantation immédiat compte tenu de l’absence de bénéfice de cette pratique (7).
Implantation d’un défibrillateur sous cutané
- En pré opératoire :
Nécessité d’un screening du patient afin de s’assurer de la bonne détection des QRS par le dispositif.
Préparation classique : dépilation, à jeun, douches bétadinées et antibioprophylaxie intra veineuse
- En per opératoire :
Sous anesthésie générale de préférence, possibilité de réaliser une implantation sous sédation vigile avec un complément par anesthésie loco régionale (Bloc Serratus).
Repérage radioguidé des sites d’incision.
Incision en regard de la xyphoïde et sur la ligne médiane axillaire gauche où est réalisée une loge en inter musculaire entre le grand dorsal et le dentelé antérieur.
Tunnelisation de la sonde entre l’incision xyphoïdienne et la loge puis entre l’incision xyphoïdienne et le haut du sternum.
Fixation de la sonde au plan profond en regard de la xyphoïde. Raccord de la sonde au boitier et fixation du boitier au plan profond de la loge.
Fermeture
Test du défibrillateur. L’étude PRAETORIAN actuellement en cours évalue la nécessité des tests de défibrillateurs sous cutanés. En attendant les résultats de cette étude, aujourd’hui en cas de contre-indication à l’induction d’une fibrillation ventriculaire (Cardiomyopathie Hypertrophique, patient très fragile…), il est possible de réaliser un choc sur l’onde R permettant de s’enquérir de l’impédance de défibrillation.
- En post opératoire
Une radiographie thoracique de face et de profil est nécessaire
Complications des défibrillateurs endocavitaires
Complications liées à l’implantation.
Elles sont similaires à celles des implantations de stimulateurs cardiaques (Infection, déplacement de sonde, hématome de loge, pneumothorax).
On note toutefois un taux plus élevé de complications. Cela est lié aux patients qui sont en général plus comorbides, à la taille des boitiers et des sondes plus importante (8).
Complications propres aux défibrillateurs
Elles sont représentées majoritairement par les thérapies inappropriées.
Les thérapies inappropriées sont liées à une mauvaise analyse des EGMs. Deux grands cas de figure sont possibles:
- Soit l’algorithme de discrimination est pris à défaut : Une tachycardie supra ventriculaire conduite rapidement aux ventricules est alors considérée comme une tachycardie ventriculaire et est traitée telle quelle.
- Soit des artéfacts (myopotentiels, interférences électro magnétiques) sont considérés comme une arythmie ventriculaire et engendre une thérapie.
Son taux annuel est estimé être entre 5 et 6% pour les défibrillateurs simple chambre et 7% pour les défibrillateurs sous cutané (9). A noter une nette amélioration ces dernières années grâce entre autres à la surveillance télécardiologique.
Les patients porteurs de défibrillateurs présentent aussi plus de complications liées aux sondes. Cela est en partie lié à la composition de ces dernières avec une fragilité accrue par rapport aux sondes de stimulateurs cardiaques. Chez les patients jeunes porteurs d’une cardiomyopathie arythmogène du ventricule droit le taux de dysfonction de sonde est évalué à 10% (10).
Suivi d’un patient porteur d’un défibrillateur
Le suivi des patients porteurs de prothèse est bien défini par des recommandations internationales (11). Actuellement, le suivi des patients porteurs de défibrillateurs est assuré à la fois par des consultations cliniques et par un suivi en télécardiologie.
Suivi clinique des patients porteurs de défibrillateurs
La consultation de contrôle d’un patient porteur d’une prothèse a quatre objectifs principaux :
1/ Évaluation du fonctionnement de la prothèse. Étape cruciale de l’interrogation, elle consiste au test des sondes et de la batterie, aux relevés des pourcentages de stimulation dans chacune des cavités ainsi qu’à la révision de la programmation.
2/ Le suivi clinique du patient. Lors de l’interrogation du dispositif, le praticien optimise la programmation selon la symptomatologie et les besoins du patient.
3/ Suivi des troubles du rythme du patient du patient. Pour cela, le praticien relève les épisodes d’arythmie et les potentielles thérapies délivrées.
4/ Éducation thérapeutique du patient porteur de prothèse.
L’interrogation d’un défibrillateur peut aujourd’hui être réalisée par un infirmier diplômé d’état et formé grâce au protocole de coopération (12; voire article sur la télésurveillance des prothèses rythmiques).
Suivi télécardiologique des patients porteurs de défibrillateurs
Révolution dans le suivi des patients porteurs de prothèses, le suivi télécardiologique occupe aujourd’hui une place centrale.
Il permet un gain de temps pour le patient et le médecin, une réduction des coûts de transport et facilite l’accessibilité aux soins.
En plus d’une surveillance calendaire, il permet une surveillance évènementielle avec alertes pour les troubles du rythme, les dysfonctions matérielles et le statut hémodynamique du patient.
La surveillance télécardiologique a prouvé un intérêt dans la réduction des chocs inapropriés et de la mortalité des patients porteurs de défibrillateurs (13;14).
Conclusion
Malgré l’amélioration constante de la prise en charge des patients insuffisants cardiaques, l’implantation de défibrillateurs garde une place centrale dans l’arsenal thérapeutique de la cardiologie. Techniquement accessible, il persiste toutefois un risque de complications per opératoires et post opératoires précoces Les chocs inappropriés et les dysfonctions de sonde représentent quant à eux la majeure partie des complications à long terme. Grâce à la télécardiologie ces dernières peuvent être prise en charge rapidement voire même dans certains cas prévenues. Les avancés technologiques récentes et à venir ont pour but de permettre encore une diminution du taux de ces complications.
Bibliographie
1. Maisel WH, Kramer DB. Implantable Cardioverter-Defibrillator Lead Performance. Circulation. 27 mai 2008;117(21):2721‑3.
2. 2019 HRS/EHRA/APHRS/LAHRS Focused Update to 2015 Expert Consensus Statement on Optimal Implantable Cardioverter-Defibrillator Programming and Testing | Heart Rhythm Society [Internet]. [cité 3 mai 2022]. Disponible sur: https://www.hrsonline.org/guidance/clinical-resources/2019-hrsehraaphrslahrs-focused-update-2015-expert-consensus-statement-optimal-implantable
3. Reduction in Inappropriate Therapy and Mortality through ICD Programming | NEJM [Internet]. [cité 3 mai 2022]. Disponible sur: https://www.nejm.org/doi/full/10.1056/NEJMoa1211107
4. Wathen MS, DeGroot PJ, Sweeney MO, Stark AJ, Otterness MF, Adkisson WO, et al. Prospective randomized multicenter trial of empirical antitachycardia pacing versus shocks for spontaneous rapid ventricular tachycardia in patients with implantable cardioverter-defibrillators: Pacing Fast Ventricular Tachycardia Reduces Shock Therapies (PainFREE Rx II) trial results. Circulation. 26 oct 2004;110(17):2591‑6.
5. 2015 ESC Guidelines for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death | European Heart Journal | Oxford Academic [Internet]. [cité 3 mai 2022]. Disponible sur: https://academic.oup.com/eurheartj/article/36/41/2793/2293363
6. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure | European Heart Journal | Oxford Academic [Internet]. [cité 3 mai 2022]. Disponible sur: https://academic.oup.com/eurheartj/article/42/36/3599/6358045
7. Healey JS, Hohnloser SH, Glikson M, Neuzner J, Mabo P, Vinolas X, et al. Cardioverter defibrillator implantation without induction of ventricular fibrillation: a single-blind, non-inferiority, randomised controlled trial (SIMPLE). The Lancet. 28 févr 2015;385(9970):785‑91.
8. Kirkfeldt RE, Johansen JB, Nohr EA, Jørgensen OD, Nielsen JC. Complications after cardiac implantable electronic device implantations: an analysis of a complete, nationwide cohort in Denmark. Eur Heart J. 7 mai 2014;35(18):1186‑94.
9. Auricchio A, Hudnall JH, Schloss EJ, Sterns LD, Kurita T, Meijer A, et al. Inappropriate shocks in single-chamber and subcutaneous implantable cardioverter-defibrillators: a systematic review and meta-analysis. EP Eur. 1 déc 2017;19(12):1973‑80.
10. Olde Nordkamp LRA, Postema PG, Knops RE, van Dijk N, Limpens J, Wilde AAM, et al. Implantable cardioverter-defibrillator harm in young patients with inherited arrhythmia syndromes: A systematic review and meta-analysis of inappropriate shocks and complications. Heart Rhythm. févr 2016;13(2):443‑54.
11. Wilkoff BL, Auricchio A, Brugada J, Cowie M, Ellenbogen KA, Gillis AM, et al. HRS/EHRA expert consensus on the monitoring of cardiovascular implantable electronic devices (CIEDs): description of techniques, indications, personnel, frequency and ethical considerations. Heart Rhythm. juin 2008;5(6):907‑25.
12. Arrêté du 7 septembre 2020 modifiant l’arrêté du 1er septembre 2020 relatif à l’autorisation du protocole de coopération « Contrôle des dispositifs implantables rythmologiques par un(e) infirmier(e) associant une prise en charge en présentiel et en télémédecine » - Légifrance [Internet]. [cité 5 mai 2022]. Disponible sur: https://www.legifrance.gouv.fr/jorf/id/JORFTEXT000042316452
13. Guédon-Moreau L, Lacroix D, Sadoul N, Clémenty J, Kouakam C, Hermida JS, et al. A randomized study of remote follow-up of implantable cardioverter defibrillators: safety and efficacy report of the ECOST trial. Eur Heart J. févr 2013;34(8):605‑14.
14. Hindricks G, Varma N, Kacet S, Lewalter T, Søgaard P, Guédon-Moreau L, et al. Daily remote monitoring of implantable cardioverter-defibrillators: insights from the pooled patient-level data from three randomized controlled trials (IN-TIME, ECOST, TRUST). Eur Heart J. 7 juin 2017;38(22):1749‑55.
Vous devez être connecté pour poster un commentaire
